干货PPT速览 医疗器械产品开发与网络技术融合全流程解析
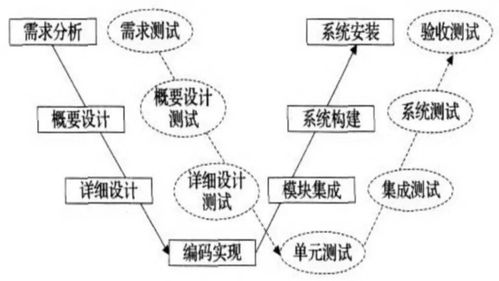
医疗器械产品开发是一个高度严谨且受法规严格监管的过程。随着网络技术的飞速发展,物联网、大数据、人工智能等新技术正深度融入医疗器械的开发周期,推动行业向智能化、远程化、个性化方向转型。以下结合PPT干货内容,系统梳理医疗器械产品开发与网络技术融合的关键流程。
一、需求分析与概念定义阶段
此阶段核心是明确临床需求与产品定位。网络技术的介入,使得开发团队能通过大数据分析海量临床数据、电子病历和公开研究,更精准地识别市场缺口与用户痛点。例如,通过分析可穿戴设备收集的连续生理参数,可为慢性病管理设备开发提供明确方向。概念定义需同步考虑产品的网络功能属性,如数据连接方式(蓝牙、Wi-Fi、5G)、云平台架构及网络安全基线。
二、法规路径规划与设计输入
医疗器械开发必须遵循各国法规(如中国NMPA、美国FDA、欧盟MDR)。集成网络技术的软件(如嵌入式软件、独立医疗软件SaMD)成为监管重点。开发团队需在早期明确产品的网络技术组件所属的合规类别(如网络安全、数据隐私GDPR/HIPAA、互操作性标准),并将其作为关键设计输入。设计输入文档需详细定义功能、性能、接口及网络安全要求(如数据加密、访问控制、安全更新机制)。
三、详细设计与技术开发
此阶段将概念转化为具体技术方案。硬件设计需考虑网络模块的集成(如低功耗芯片、天线设计)。软件开发成为重心,包括:
- 嵌入式开发:实现设备端的网络连接、数据采集与本地处理。
- 云端与后端开发:构建安全可靠的云平台,用于数据存储、分析、可视化及远程管理。微服务架构、API设计是关键。
- 移动端/Web端应用开发:提供用户(医护或患者)交互界面。
- 网络安全贯穿始终:实施威胁建模、安全编码、漏洞测试,确保数据在传输与存储中的机密性、完整性和可用性。
四、原型构建与设计验证
制作集成网络功能的工程原型,通过严格的测试验证设计是否满足输入要求。测试重点包括:
- 功能与性能测试:网络连接稳定性、数据传输速率与延迟、多设备并发能力。
- 网络安全测试:渗透测试、漏洞扫描、数据加密验证。
- 互操作性测试:与医院信息系统(HIS、EMR)或其他设备的标准接口(如HL7、FHIR、DICOM)对接测试。
五、设计确认与临床评价
通过临床评价(可能包括临床试验)确认产品在真实使用环境下的安全有效性。网络技术在此阶段发挥巨大价值:远程监控功能可简化临床试验数据收集;真实世界数据(RWD)可作为临床证据的补充。必须验证网络功能在临床场景下的可靠性与安全性。
六、注册申报与质量管理体系
整理技术文档,提交监管机构注册/申报。对于含网络技术的产品,需额外提交网络安全文档、架构描述、风险控制措施等。整个开发过程必须在完善的质量管理体系(如ISO 13485)下进行,确保开发过程可追溯、可控制。软件生命周期过程需遵循IEC 62304标准。
七、生产转移与上市后监管
产品获批后,转入规模化生产。网络技术部分(特别是软件)需建立持续维护机制,包括:
- 远程监控与维护:通过网络对已部署设备进行状态监控、故障诊断和软件更新。
- 网络安全漏洞管理:建立应急响应机制,持续监控和修补新发现的安全漏洞。
- 数据迭代与产品优化:利用收集的匿名化大数据,分析产品性能,为下一代产品开发提供洞察。
****
网络技术已深度嵌入医疗器械产品开发的全链条,从需求洞察到上市后生命周期管理。成功的开发需要跨学科团队(医学、工程、软件、网络安全、法规)紧密协作,并始终将网络安全、数据隐私和法规合规置于核心地位。拥抱网络技术,不仅能开发出更智能、高效的医疗器械,更能构建以数据为驱动的连续健康服务生态。
如若转载,请注明出处:http://www.xyycwlkj.com/product/79.html
更新时间:2026-05-29 09:22:37